Do zespołu Cushinga może prowadzić zmiana aktywności osi podwzgórze – przysadka – nadnercza, za objawy kliniczne odpowiada podwyższone stężenie kortyzolu we krwi, które prowadzi do zaburzenia równowagi wewnętrznej ustroju.
Medme poleca
Zespół Cushinga - co to jest?
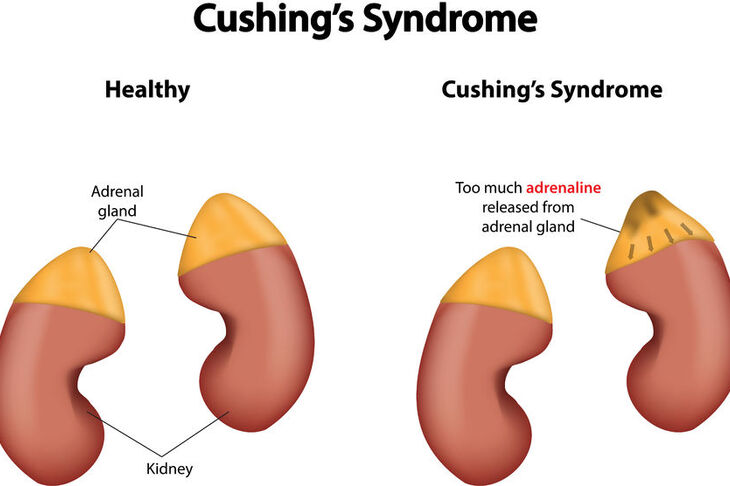
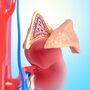
Zespół Cushinga to zespół objawów klinicznych wynikających z podwyższonego stężenia glikokortykosteroidów w ustroju. Glikokortykosteroidy (GKS) to hormony produkowane przez korę nadnerczy - parzystego narządu położonego na górnych biegunach nerek.
Najważniejszym z nich jest kortyzol, który poprzez wpływ na przemiany metaboliczne:
- białek,
- tłuszczów,
- węglowodanów
zapewnia utrzymanie równowagi wewnętrznej organizmu, prawidłowe gojenie się ran oraz umożliwia adaptację do sytuacji stresowych.
Wydzielanie glikokortykosteroidów przez korę nadnerczy regulowane jest przez przysadkę mózgową. Produkuje ona hormon o nazwie adrenokortykotropina – ACTH – który pobudza nadnercza do produkcji kortyzolu. Ponieważ ilość uwalnianego ACTH zmienia się w ciągu doby, również stężenie kortyzolu wykazuje dobowe wahania – w prawidłowych warunkach jest maksymalne w godzinach porannych, a minimalne około północy. Aktywność przysadki podlega natomiast kontroli podwzgórza, które produkuje kortykoliberynę – CRH – hormon uwalniający ACTH z przysadki. Cały ten układ działa w mechanizmie sprzężenia zwrotnego ujemnego. Oznacza to, że wysokie stężenie kortyzolu hamują produkcję ACTH i CRH, a niskie stężenie zwiększa produkcję tych hormonów.
Reklama
Zespół Cushinga - przyczyny
Przyczyny prowadzące do rozwoju zespołu Cushinga są podstawą jego podziału na następujące typy:
- Egzogenny – czyli spowodowany podażą glikokortykosteroidów z zewnątrz. Jest następstwem długotrwałego stosowania steroidów w celach terapeutycznych w wielu jednostkach chorobowych. Z punktu widzenia epidemiologii ta przyczyna zespołu Cushinga jest najczęstsza.
- Endogenny – kortyzol produkowany jest przez organizm w ilościach większych niż fizjologiczne. W tym typie zespołu Cushinga możemy wyróżnić dwie główne grupy:
1. Zespół Cushinga ACTH-zależny – zwiększone wytwarzanie kortyzolu przez nadnercza wynika z wzmożonej produkcji ACTH. Najczęstszą przyczyną (80%) jest obecność gruczolaka przysadki mózgowej, wydzielającego ACTH. Gruczolak to nowotwór łagodny, w 90% przypadków ma małe rozmiary (mikrogruczolak). Gruczolaki o rozmiarach większych niż 10 mm (makrogruczolaki) występują dużo rzadziej. Stan, w którym objawy zespoły Cushinga spowodowane są gruczolakiem przysadki produkującym ACTH, nazywamy chorobą Cushinga. Roczną zapadalność szacuje się na 0,1 – 1/100 000. Kobiety chorują 8 razy częściej niż mężczyźni.
Inną przyczyną ACTH–zależnego zespołu Cushinga może być uwalnianie ACTH przez guzy umiejscowione poza przysadką mózgową, tzw. zespół ekotopowego wydzielania ACTH. Hormon ten najczęściej produkowany jest przez raka drobnokomórkowego płuc, ale także nowotwory jelit, grasicy, trzustki lub jajnika.
2. Zespół Cushinga ACTH – niezależny – wzrost produkcji kortyzolu jest wynikiem nadaktywności samych nadnerczy, która może być spowodowana obecnością guzów lub zmian rozrostowych.
U osób dorosłych najczęstszym guzem nadnerczy, który może samodzielnie produkować kortyzol, jest gruczolak. U dzieci natomiast najczęściej występuje rak nadnerczy. Zmiany rozrostowe oznaczają, że wzrost masy nadnerczy przybiera mniej ograniczoną, zorganizowaną formę niż w przypadku guza. Ze względu na strukturę zmiany, rozrost może być typu makro- lub mikroguzkowego. Rozrost makroguzkowy wynika z nietypowego pobudzania kory nadnerczy do wzrostu przez różne hormony produkowane m.in. w przewodzie pokarmowym, jajnikach i przysadce mózgowej (GIP, estrogeny, FSH, LH). Rozrost mikroguzkowy ma podłoże genetyczne.
Istnieje jeszcze trzeci typ zespołu Cushinga, tzw. rzekomy. Zespół Cushinga może czasem być związany z:
- depresją
- jadłowstrętem psychicznym,
- alkoholizmem.
Podstawowym czynnikiem prowadzącym do rozwoju egzogennej postaci zespołu Cushinga jest stosowanie preparatów zawierających hormony glikokortykosterydowe (tabletki, maści, inhalacje, zastrzyki). Podaje się je w leczeniu chorób dermatologicznych, autoimmunologicznych, po przeszczepach i w wielu innych sytuacjach klinicznych. Pojawienie się objawów zespołu Cushinga wymaga rozważenia zmiany dawkowania lub alternatywnej metody leczenia, jeśli taka istnieje.
Reklama
Zespół Cushinga - objawy
Do zespołu Cushinga może prowadzić zmiana aktywności osi podwzgórze – przysadka – nadnercza na którymkolwiek z poziomów, jednak niezależnie od przyczyny, za objawy kliniczne odpowiada podwyższone stężenie kortyzolu we krwi, które prowadzi do zaburzenia równowagi wewnętrznej ustroju.
Do charakterystycznych objawów zalicza się:
- charakterystyczna sylwetka, wynikająca z odkładania się tkanki tłuszczowej w okolicy tułowia, karku i twarzy, ze stosunkowo szczupłymi kończynami - twarz chorych z ZC jest zaokrąglona, często zaczerwieniona (twarz księżycowata), szyja krótka i szeroka (bawoli kark),
- cienka skóra z purpurowymi rozstępami, głownie na skórze brzucha, bioder, pośladków, ud, sutków - są one następstwem aktywacji przez GKS enzymów osłabiających tkankę łączną, która buduje skórę,
- skłonność do siniaczenia, tworzenia samoistnych wylewów krwawych do skóry oraz wybroczyn,
- podatność na urazy skóry i opóźnione gojenie ran,
- osłabienie oraz zanik mięśni kończyn i tułowia, zła tolerancja wysiłku fizycznego, dużemu zanikowi ulegają mięśnie obręczy barkowej i miednicznej, co skutkuje trudnościami z chodzeniem po schodach, wstawaniem z krzesła, itp.,
- skłonność do złamań kości wynikająca z osteoporozy, narażone są głównie żebra, trzony kręgów oraz kości tworzące miednicę (kości łonowe i kulszowe),
- zwiększone pragnienie i wielomocz (objawy nieprawidłowej tolerancji glukozy),
- wzrost apetytu,
- przyrost masy ciała,
- bóle i zawroty głowy, wynikające z nadciśnienia tętniczego, obecnego w 70-80% przypadków,
- objawy choroby niedokrwiennej serca, której rozwój jest przyspieszony w ZC (bóle zamostkowe o charakterze ucisku, związane najczęściej z wysiłkiem fizycznym lub stresem),
- objawy choroby wrzodowej żołądka i dwunastnicy oraz kamicy nerkowej,
- zaburzenia widzenia z powodu rozwijającej się jaskry lub zaćmy,
- skąpe krwawienia miesięczne lub brak miesiączki u kobiet oraz osłabienie potencji u mężczyzn,
- obniżenie odporności objawiające się skłonnością do infekcji; szczególnie częste są zakażenia grzybicze,
- zaburzenia emocjonalne, tj. euforia lub depresja, rozdrażnienie, niepokój, zaburzenia snu, zaburzenia pamięci, w skrajnych przypadkach psychozy i skłonności samobójcze,
- w niektórych przypadkach ZC wysokiemu stężeniu kortyzolu towarzyszy nadmiar androgenów; pojawia się wówczas trądzik, a u kobiet owłosienie typu męskiego (tzw. hirsutyzm).
Reklama
Zespół Cushinga - konsultacja lekarska
Każdy z wymienionych objawów wymaga szybkiej konsultacji lekarskiej z kilku powodów.
- Szybka diagnoza umożliwia wczesne rozpoczęcie leczenia, co zapobiegnie pogłębieniu choroby i pojawieniu się nowych objawów.
- Objawy zespołu Cushinga mogą wynikać z obecności nowotworu produkującego ACTH (np. rak drobnokomórkowy płuc) – taka ewentualność wymaga sprawnej diagnostyki.
- Wiele objawów pojawiających się w zespole Cushinga, występuje też w innych jednostkach chorobowych (wahania nastroju w zaburzeniach psychiatrycznych, skłonność do siniaczenia w niektórych postaciach skaz krwotocznych).
- Część objawów tego zespołu może też stanowić odrębne jednostki chorobowe (nadciśnienie tętnicze, cukrzyca, osteoporoza).
Wizyta u lekarza jest więc wysoce wskazana w przypadku zaobserwowania któregokolwiek z nich, w celu ustalenia ich przyczyny.
U podstaw zespołu Cushinga leży zaburzenie stężenia hormonów, stąd pacjent, który zaobserwuje u siebie objawy budzące podejrzenie tej choroby, powinien udać się do endokrynologa. Aby lepiej zrozumieć swój problem, przed wizytą u lekarza pacjent powinien zasięgnąć informacji ze źródeł medycznych (dostępnych w podręcznikach, poradnikach, Internecie) na temat istoty swojej choroby i sposobów radzenia sobie z nią. Ułatwi to zrozumienie sugestii lekarza co do postępowania terapeutycznego oraz umożliwi świadomą współpracę.
Pomocne może być znalezienie odpowiedzi na kilka podstawowych pytań:
- Co to jest zespół Cushinga?
- Jakie są przyczyny ZC?
- Które narządy zostają uszkodzone w ZC?
- Jakie są jego objawy?
- Które z objawów są najbardziej niepokojące?
- Czy wszystkie objawy ustępują w wyniku leczenia?
- Jakie badania diagnostyczne należy wykonać, aby rozpoznać ZC?
- Jak przygotować się do tych badań?
- Na czym polega leczenie ZC?
- Czy konieczna jest hospitalizacja?
- Czy zespół Cushinga jest całkowicie uleczalny?
- Czy występują nawroty?
- Czy są jakieś czynniki wywołujące ZC?
- Czy można zmniejszyć nasilenie objawów domowymi sposobami?
- Czy zespół Cushinga to choroba dziedziczna?
- Czy pacjentka z ZC może zajść w ciążę?
- Czy ZC może być wskaźnikiem obecności innego procesu chorobowego w organizmie?
Oczywiście odnalezienie odpowiedzi na wszystkie pytania w literaturze jest trudne. Jeśli jednak pacjent będzie posiadał choćby podstawową wiedzę na temat zespołu Cushinga przed wizytą u lekarza, uzyskanie informacji co do bardziej szczegółowych aspektów tej choroby już bezpośrednio podczas konsultacji będzie o wiele łatwiejsze.
Reklama
Hormony glikokortykosteroidy - jakie mają działanie?
Glikokortykosteroidy (GKS) to hormony, które wpływają na przemiany wszystkich głównych grup związków w organizmie człowieka, a więc białek, tłuszczów i węglowodanów, jak również na gospodarkę wodno–elektrolitową. Nieprawidłowe ich stężenie prowadzi do zaburzeń wielu procesów metabolicznych oraz patologii licznych narządów.
Skóra
Wysokie stężenie GKS nasila rozpad białka, podstawowego składnika budującego strukturę tkanek i narządów. Aktywuje też enzymy rozkładające składniki tkanki łącznej, tworzącej skórę. Skóra staje się:
- cienka,
- podatna na urazy, których gojenie jest utrudnione,
- pokryta w rozstępy, których purpurowa barwa wynika z prześwitywania naczyń krwionośnych,
- skłonna do siniaczenia - jest to spowodowane kruchością naczyń krwionośnych.
Tkanka podskórna
GKS zmieniają rozmieszczenie tkanki tłuszczowej. Z typowych miejsc występowania (uda, pośladki, piersi u kobiet) tłuszcz zostaje przeniesiony bliżej osi ciała (twarz, szyja, tułów), stąd charakterystyczna dla zespołu Cushinga otyłość centralna. Główną przyczyną otyłości jest jednak pobudzenie apetytu przez GKS.
Mięśnie
Osłabienie i zanik mięśni wiąże się z nasilonym rozpadem białek oraz niedoborem potasu i fosforanów, których zwiększone ilości wydalane są z moczem.
Kości
Kortyzol w wysokich stężeniach powoduje rozkład macierzy kostnej oraz niedobór wapnia (zmniejszenie wchłaniania wapnia w przewodzie pokarmowym i zwiększone wydalanie wraz z moczem). Hamuje również działanie hormonu wzrostu w kościach. Skutkiem jest zmniejszenie gęstości tkanki kostnej i częste złamania. Patologiczna łamliwość kości w ZC to również skutek nadmiernego ich obciążenia wynikającego z otyłości.
Układ krążenia
Przewlekle podwyższone stężenie kortyzolu prowadzi do rozwoju nadciśnienia tętniczego w 70-80% ZC. Kortyzol w dużych dawkach powoduje zatrzymanie wody i sodu w organizmie, co zwiększa objętość krążącej krwi. Nasila też działanie substancji obkurczających naczynia krwionośne (katecholaminy, endotelina). Oba te mechanizmy podnoszą ciśnienie krwi.
GKS podwyższają stężenie cholesterolu i trójglicerydów we krwi, co w połączeniu z nadciśnieniem tętniczym przyspiesza rozwój miażdżycy. Blaszki miażdżycowe odkładające się w naczyniach wieńcowych zmniejszają przepływ krwi przez mięsień sercowy, co skutkuje przyspieszonym rozwojem choroby niedokrwiennej serca.
Układ pokarmowy
Steroidy nadnerczowe powodują nadżerki i owrzodzenia w błonie śluzowej żołądka i dwunastnicy, dając dolegliwości choroby wrzodowej. Jest to szczególnie częste wśród pacjentów przyjmujących równocześnie niesterydowe leki przeciwzapalne.
Układ moczowo-płciowy
Kortyzol powoduje wydalanie z moczem zwiększonych ilości wapnia, co przyczynia się do powstawania złogów wapniowych i kamicy nerkowej.
Duże stężenie steroidów hamuje wydzielanie hormonów przysadki i podwzgórza, odpowiedzialnych za regulację funkcji jajników i jąder. Skutkiem jest zmniejszenie ilości estrogenów i testosteronu, które u kobiet przejawia się skąpymi miesiączkami lub ich brakiem, a u mężczyzn spadkiem potencji.
Układ nerwowy
Receptory dla kortyzolu znajdują się również w mózgu, dlatego jego nieprawidłowe stężenie prowadzi do niestabilności emocjonalnej i zaburzeń psychicznych. Często pacjenci z ZC trafiają najpierw do psychiatry, zanim zostanie wykryta przyczyna ich problemów.
Układ odpornościowy
GKS zmniejszają liczbę limfocytów B oraz limfocytów T, które odpowiadają za dwa podstawowe typy reakcji odpornościowych – humoralną i komórkową. Prowadzi to do częstych infekcji, w tym zakażeń drobnoustrojami, które u zdrowych osób nie wywołują objawów choroby (tzw. zakażenia oportunistyczne).
Trzustka
Kortyzol jest hormonem wydzielanym prawidłowo w warunkach stresu. Jego funkcja polega między innymi na dostarczeniu komórkom glukozy, której zużycie jest wtedy zwiększone. Utrzymujące się przewlekle podwyższone stężenie kortyzolu we krwi prowadzi do ciągłej hiperglikemii, a więc wysokiego stężenia glukozy we krwi. W odpowiedzi na taki stan, komórki wysp Langerhansa w trzustce produkują insulinę, która ma za zadanie to stężenie obniżyć. Jednak jeżeli hiperglikemia jest długotrwała, z czasem trzustka nie jest w stanie wydzielać wystarczającej ilości insuliny - rozwija się cukrzyca. Dodatkowym mechanizmem prowadzącym do rozwoju cukrzycy jest insulinooporność, będąca następstwem otyłości. Duża zawartość tkanki tłuszczowej w organizmie sprawia, że tkanki nie reagują na insulinę. Z rozwojem cukrzycy wiąże się zwiększone pragnienie i wielomocz.
Reklama
Zespół Cushinga - diagnostyka
Postacie endogenne (wewnętrzne) zespołu Cushinga, jak sama nazwa wskazuje, nie mają wyraźnego związku z oddziaływaniami zewnętrznymi i trudno w tych przypadkach wskazać czynniki ryzyka rozwoju choroby.
Przed rozpoczęciem pełnej diagnostyki należy wykluczyć najprostszą przyczynę zespołu Cushinga, a więc przyjmowanie przez pacjenta leków zawierających preparaty sterydowe. Rozpoznanie zespołu Cushinga można postawić na podstawie charakterystycznych objawów klinicznych oraz zmian w badaniach biochemicznych. Należy w tym miejscu zaznaczyć, że w większości przypadków ZC na początku występuje tylko kilka objawów (np. nadciśnienie, cukrzyca, otyłość typu centralnego). Pełnoobjawowy zespół spotykany jest tylko w zaawansowanych stadiach choroby. Stąd konieczna jest czujność pacjenta oraz lekarza, aby uchwycić wczesne symptomy choroby i wykonać badania laboratoryjne, które ostatecznie potwierdzą jej obecność.
1. Badanie dobowego wydalania kortyzolu z moczem - wynik tego badania odzwierciedla stężenie kortyzolu we krwi w danym przedziale czasowym, a więc umożliwia zdiagnozowanie hiperkoryzolemii (podwyższone stężenie kortyzolu we krwi), leżącej u podstaw zespołu Cushinga.
Badanie wymaga przeprowadzenia przez pacjenta dobowej zbiórki moczu. Oznacza to, że przez 24 godziny pacjent oddaje każdą porcję moczu do pojemnika, a zebrana w ten sposób objętość moczu zostanie następnie poddana badaniu na ilość zawartego kortyzolu.
Wymaga to od pacjenta pewnej dyscypliny, gdyż jest niezwykle istotne, aby badaniu została poddana cała objętość moczu oddanego w ciągu doby. W warunkach szpitalnych można przeprowadzić dobową zbiórkę moczu, zakładając pacjentowi cewnik do pęcherza moczowego, co znacznie ułatwia procedurę. 3-4-krotne przekroczenie górnej granicy normy zawartości kortyzolu potwierdza jednoznacznie rozpoznanie zespołu Cushinga.
Wynik, który przekracza górną granicę normy mniej niż 3 razy jest wątpliwy.
Może być spowodowany:
- przewlekłym stresem,
- alkoholizmem,
- depresją,
- ciążą.
Prawidłowy wynik uzyskany w pojedynczym badaniu nie wyklucza ZC, dlatego przy uzyskaniu takiego wyniku dobową zbiórkę moczu należy powtórzyć jeszcze dwa razy.
2. Badanie stężenia kortyzolu w surowicy - badanie wymaga pobrania krwi rano i wieczorem, a u osób hospitalizowanych można również pobrać krew około północy. Dla zespołu Cushinga charakterystyczne jest zniesienie dobowego rytmu wydzielania kortyzolu. Brak jest zmniejszania się stężenia hormonu w godzinach popołudniowych, wieczornych i nocnych.
3. Test hamowania małą dawką deksametazonu - deksametazon to syntetyczny hormon sterydowy, który silnie hamuje wydzielanie ACTH przez przysadkę i CRH przez podwzgórze. W prawidłowych warunkach jego podanie zmniejsza stężenie tych hormonów, a w konsekwencji stężenie kortyzolu. Badanie polega na podaniu pacjentowi doustnie 1 mg deksametazonu przed snem (około godziny 23.00), a następnie pobraniu krwi między godziną 8.00 a 9.00 następnego dnia i oznaczeniu ilości kortyzolu. W zespole Cushinga nie stwierdza się odpowiedniego zmniejszenia stężenia kortyzolu we krwi. Czasem wynik tego badania może być również dodatni u osób bez ZC, ale będących w stanie przewlekłego stresu, depresji, przyjmujących leki przeciwpadaczkowe lub doustne środki antykoncepcyjne.
Reklama
Zespół Cushinga - badania
Po rozpoznaniu zespołu Cushinga należy znaleźć jego przyczynę. W tym celu wykonywane są następujące badania:
1. Oznaczanie stężenia ACTH w surowicy krwi - badanie pozwala na zróżnicowanie między dwoma głównymi rodzajami zespołu Cushinga, tj. ZC ACTH–zależnym i ACTH–niezależnym. Jeżeli stężenie ACTH w próbce krwi pobranej o godzinie 9.00 jest niskie (< 2 pmol/l), wskazuje to na ZC ACTH-niezależny; jeżeli jest wysokie (> 4 pmol/l) – na ZC zależny od ACTH. Wartości pośrednie są niejednoznaczne i wymagają wykonania kolejnego testu – tzw. testu stymulacyjnego z CRH.
2. Test stymulacyjny z CRH - badanie ma pokazać, w jaki sposób podwzgórzowy hormon CRH wpływa na wydzielanie przysadkowego ACTH. W tym celu bada się stężenie ACTH we krwi, wstrzykuje się dożylnie 100 ug syntetycznego CRH, a następnie znów bada się stężenie ACTH po 15, 30, 60 i 90 minutach od podania CRH. W zespole Cushinga ACTH–zależnym CRH powoduje znaczący wzrost stężenia ACTH. W ZC ACTH–niezależnym taki wzrost nie występuje.
3. Test hamowania dużą dawką deksametazonu - badanie to jest szczególnie istotne dla zróżnicowania przyczyn zespołu Cushinga zależnego od ACTH, a więc dla stwierdzenia, czy jest on spowodowany gruczolakiem przysadki mózgowej (choroba Cushinga) czy też zespołem ektopowego wydzielania ACTH (np. przez guz nowotworowy). Polega na oznaczeniu stężenia kortyzolu we krwi o godzinie 8.00, a następnie na podaniu pacjentowi doustnie 8 mg deksametazonu o godzinie 23.00. Następnego dnia o godzinie 8.00 ponownie oznacza się stężenie kortyzolu. Jeżeli przyczyną zespołu Cushinga jest nadprodukcja ACTH przez przysadkę (choroba Cushinga), w drugim dniu testu uzyskuje się zmniejszenie stężenia kortyzolu o połowę. Jeżeli przyczyną jest ektopowe wydzielanie ACTH, zwykle nie dochodzi do obniżenia stężenia kortyzolu.
Po wykonaniu badań laboratoryjnych kolejnym krokiem do potwierdzenia rozpoznania jest przeprowadzenie odpowiednich badań obrazowych. Jeżeli badania laboratoryjne wskazują na postać ZC niezależną od ACTH, przyczyny podwyższonego stężenia kortyzolu należy poszukiwać w nadnerczach. Stąd konieczne jest wykonanie obrazowania nadnerczy w poszukiwaniu guza lub rozrostu.
Najprostszym i najmniej inwazyjnym badaniem, służącym do wstępnej oceny nadnerczy, jest badanie ultrasonograficzne (USG). Przeprowadza się je na czczo, tzn. pacjent nie powinien 8 godzin przed badaniem:
- przyjmować pokarmów,
- napojów (zwłaszcza gazowanych),
- palić papierosów.
Dokładniejszej oceny nadnerczy można dokonać za pomocą:
- tomografii komputerowej (TK),
- rezonansu magnetycznego (MRI).
Wykonanie TK wiąże się z dożylnym podaniem środków kontrastowych, trzeba zachować więc szczególną ostrożność u alergików, szczególnie, jeśli w przeszłości wystąpiła reakcja alergiczna na środki kontrastowe. MRI jest pod tym względem badaniem bezpieczniejszym, gdyż stosowana tu substancja kontrastująca rzadziej wywołuje reakcje uczuleniowe.
MRI nie można z kolei wykonać u osób z rozrusznikiem serca oraz jakimikolwiek metalowymi elementami obecnymi w ciele na stałe:
- protezy,
- niektóre rodzaje plomb dentystycznych,
- tatuaże.
Tomografia komputerowa oraz rezonans magnetyczny również powinny być wykonane na czczo.
Jeżeli wyniki badań biochemicznych wskazują natomiast na zespół Cushinga zależny od ACTH, należy skoncentrować się na badaniach obrazowych przysadki mózgowej, gdyż 80% ACTH–zależnego ZC stanowi choroba Cushinga, czyli gruczolak przysadki produkujący ACTH. Najczęściej ujawnienie w tomografii komputerowej lub rezonansie magnetycznym guza przysadki potwierdza rozpoznanie choroby Cushinga.
Jeśli jednak mimo stwierdzenia guza przysadki obraz kliniczny jest niejednoznaczny, to znaczy istnieją pewne objawy sugerujące obecność toczącego się w organizmie procesu nowotworowego, należy poszukać przyczyn wysokiego stężenia kortyzolu również poza przysadką mózgową. Może się bowiem zdarzyć, że ujawniony w obrazowaniu guz to tzw. incydentaloma, czyli guz występujący u >10% zdrowych osób, który nie ma nic wspólnego z nadprodukcją ACTH, a prawdziwa przyczyna nadmiaru tego hormonu leży w guzach ektopowo wydzielających ACTH. W celu ich wykrycia przeprowadza się tomografię komputerową klatki piersiowej i brzucha. Pomocna może być również scyntygrafia receptorowa – metoda wykrywająca za pomocą izotopów komórki nowotworowe produkujące hormony.
Czasem zróżnicowanie, czy nadprodukcja ACTH wynika z guza przysadki czy guza pozaprzysadkowego jest wyjątkowo trudne i wymaga zacewnikowania zatok żylnych w okolicach przysadki mózgowej, aby pobrać krew z bezpośredniego sąsiedztwa przysadki i zbadać w niej stężenie ACTH. Jeżeli jest ono >2 razy większe niż stężenie we krwi pobranej z ramienia, wskazuje to na obecność guza przysadki.
Diagnostykę zespołu ektopowej produkcji ACTH należy oczywiście wykonać również wtedy, gdy badania laboratoryjne wskazują na ACTH-zależny ZC, a badania obrazowe nie ujawniają guza przysadki.
W przypadku zespołu Cushinga wywołanego podawaniem leków sterydowych należy rozważyć stopniowe zmniejszanie dawki leku lub jego odstawienie (o ile jest to możliwe).
Zespół Cushinga - leczenie
Leczenie pozostałych przypadków zespołu Cushinga polega na operacyjnym usunięciu przyczyny nadmiaru kortyzolu w organizmie.
Gruczolak przysadki
Chirurg przez nos dostaje się do przysadki mózgowej i w sposób selektywny usuwa gruczolaka, pozostawiając zdrową tkankę. O skuteczności operacji świadczy normalizacja stężenia ACTH. W razie braku skuteczności zabiegu lub nawrotu choroby zaleca się powtórną operację lub radioterapię okolic przysadki. Skuteczność leczenia operacyjnego sięga 90 % i prowadzi do ustąpienia objawów zespołu Cushinga.
Przygotowanie do operacji poprzedzone jest leczeniem farmakologicznym, które ma zmniejszyć powikłania związane z nadmiarem kortyzolu, jak:
- krwawienia śródoperacyjne,
- zakażenia,
- powikłania zakrzepowo-zatorowe.
Polega ono na podawaniu leków hamujących wytwarzanie sterydów nadnerczowych, tj. ketokonazol, metyrapon lub mitotan. Taka terapia ułatwia również leczenie cukrzycy i nadciśnienia tętniczego.
Zespół ektopowej produkcji ACTH
Leczenie polega na operacyjnym usunięciu pierwotnego guza produkującego ACTH. Podobnie jak w przypadku gruczolaka przysadki zabieg poprzedzony jest leczeniem farmakologicznym. W przypadku guzów łagodnych ich usunięcie prowadzi do całkowitego wyleczenia. W przypadku guzów złośliwych konieczna jest również radioterapia. Część nowotworów jest nieoperacyjna - wówczas metodą leczniczą pozostaje radioterapia, chemioterapia oraz podawanie substancji hamujących wytwarzanie sterydów nadnerczowych. Rokowane zależy od rodzaju pierwotnego guza i stadium jego zaawansowania.
Guz nadnercza
Leczeniem z wyboru jest operacyjne usunięcie guza, poprzedzone zastosowaniem leków hamujących wytwarzanie hormonów sterydowych. Należy je podawać z dużą ostrożnością, gdyż niektóre guzy nadnerczy bardzo silnie na nie odpowiadają; w skrajnych przypadkach może dojść do całkowitego zahamowania produkcji kortyzolu i wystąpienia ostrej niewydolności kory nadnerczy (tzw. przełom nadnerczowy), który jest stanem zagrażającym życiu. Obecność guza nadnercza wydzielającego duże ilości kortyzolu sprawia, że tkanka drugiego, zdrowego nadnercza zanika i zaraz po operacji nie jest w stanie wytwarzać wystarczającej ilości tego hormonu. W trakcie operacji podaje się więc sterydy nadnerczowe, aby po usunięciu guza nie doszło do niebezpiecznego spadku jego stężenia kortyzolu. Stosowanie hydrokortyzonu może być konieczne do dwóch lat po operacji - tyle bowiem może trwać podjęcie normalnej funkcji przez drugie nadnercze.
Usunięcie gruczolaka nadnerczy powoduje ustąpienie objawów chorobowych w ciągu 4-5 tygodni. Jedynie w przypadku długiego czasu trwania choroby mogą wystąpić powikłania naczyniowe wynikające z nadciśnienia tętniczego. W przypadku raka nadnerczy leczenie pooperacyjne i rokowanie zależą od stopnia zaawansowania nowotworu.
Rozrost guzkowy nadnerczy
Metodą leczniczą jest obustronne usunięcie nadnerczy (jednocześnie lub dwuetapowo). Podobnie jak w operacji usunięcia gruczolaka nadnercza konieczna jest osłona sterydowa w czasie operacji. Po zabiegu niezbędne jest stałe leczenie zastępcze hydrokortyzonem. Usunięcie zmienionych chorobowo nadnerczy powoduje ustąpienia objawów zespołu Cushinga.
Zespół Cushinga - pobyt w szpitalu
Jak wynika z opisu przedstawionych metod, leczenie zespołu Cushinga wymaga hospitalizacji w oddziale endokrynologicznym, a następnie chirurgicznym. Przynosi dobre rezultaty, gdyż usunięcie przyczyny nadmiaru kortyzolu z reguły prowadzi do ustąpienia licznych objawów tego zespołu chorobowego.
Objawy zespołu Cushinga w większości ustępują w wyniku leczenia przyczynowego, stąd zadaniem pacjenta i lekarza jest ich wczesne zauważenie i przeprowadzenie odpowiedniej diagnostyki oraz terapii. Ważna jest edukacja, aby chory miał świadomość, że z pozoru niezwiązane ze sobą objawy (np. osteoporoza, zmiany psychiczne i łatwe siniaczenie) mają wspólną przyczynę, której usunięcie w krótkim czasie powoduje ich ustąpienie. W niektórych przypadkach po operacji konieczne jest stałe doustne przyjmowanie hydrokortyzonu, co wymaga od pacjenta pewnej dyscypliny.
Zespół Cushinga może być powikłaniem leczenia preparatami zawierającymi sterydy nadnerczowe, które stosowane są w wielu jednostkach chorobowych. W takiej sytuacji pacjent powinien uzyskać od lekarza informacje, czy istnieje w ogóle możliwość odstawienia sterydów lub zmniejszenia ich dawki, czy można stosować inne leki dające podobne efekty terapeutyczne, czy działania niepożądane w postaci zespołu Cushinga nie są bardziej uciążliwe i szkodliwe niż pierwotna choroba, a następnie wybrać wraz lekarzem optymalną drogę leczenia.